lunes, 20 de octubre de 2014
lunes, 8 de septiembre de 2014
lunes, 23 de junio de 2014
Ejercicios de ejemplo
1. 1) En relación a los isómeros:
a.
Defínelos
b.
Cuantos isómeros estructurales
tiene el C5H12? Representa las formulas desarrolladas y nómbralos.
c.
Formula y nombra los isómeros de C5H12O.
1. 2) Se realiza la combustión
completa del Etanol.
a.
Escribe la ecuación de esta reacción
química (igualada)
b.
Indica los moles y gramos que
reaccionan para reactivos y productos.
c.
Cuántos moles de oxigeno
reaccionan con 0,5 moles de etanol?
d.
A cuantos gramos y moléculas
corresponde la parte c?
e. Cuántos
gramos de agua puedo obtener si reaccionan completamente 3 moles de etanol con
oxígeno el necesario para que se produzca una combustión completa.
3) En relación a los isómeros:
a) Qué son y que tipos conoce. B) Explica si los siguientes compuestos son
isómeros entre sí y clasificalos: i) butano
ii) metilpropano iii)
ciclobutano iv) 2-propanol v) 2-buteno
vi) 1-propanol.
4) En relación a los glúcidos:
a) Mencione sus principales características (cite ejemplos). b) la glucosa es
un importante glúcido para los seres vivos dada su función energética, que es
posible gracias a la siguiente reacción. A) Nombra la reacción, los componentes
e iguala. B) realiza un cuadro que
indique el número de moles y masa molar de los compuestos. C) ¿Cuántos moles de oxígeno se precisan
para “quemar” completamente 60g de glucosa? C6H12O6 +
O2 --------à CO2
+ H20 + ENERGÍA
5) En relación a las soluciones: a) Explica
qué son y cómo se las puede clasificar
b) ¿Qué solución de agua y sal común (NaCl) está más
concentrada? Fundamenta con cálculos.
| i) 1 mol NaCl, 100 ml solución ii) 35g NaCl, 0,050ml solución |
|||||||
sábado, 24 de mayo de 2014
Propiedades de los Compuestos
Orgánicos
Propiedades Físicas
|
||||||||||||||||
Alcanos
|
Alquenos
|
Alquinos
|
Benceno
|
|||||||||||||
Estado Físico
|
Desde C1 hasta C4 gases,
desde C5 hasta C17 líquidos y desde C18 en adelante
sólidos.
|
Tres primeros miembros son gases, del C5
hasta el C18 son líquidos y los demás
sólidos
|
Son gases hasta el C5, líquidos
hasta el C15 y luego sólidos
|
Es un líquido a temperatura
ordinaria, incoloro y con olor aromático.
|
||||||||||||
P. Ebullición
|
Aumento constante al aumentar el
número de átomos de carbono
|
Un poco más bajos que los
alcanos.
|
Más altos que los de los
correspondientes alquenos y alcanos
|
|||||||||||||
P. Fusión
|
alternancia a medida que se progresa de
un alcano con un número par de átomos de C,
al siguiente con un número impar de átomos de
C
|
Ligeramente mayores que el de los
alcanos
|
Más altos que los de los
correspondientes alquenos y alcanos
|
|||||||||||||
Densidad
|
Menor a 1g/mL, (la densidad
del agua a
4°C).
|
Un poco más alta que la de los
alcanos
|
Más altos que los de los
correspondientes alquenos y alcanos
|
Su densidad es de 0,874 g/mL a 20°C,
más liviano que el agua.
|
||||||||||||
Solubilidad
|
Casi totalmente insolubles en agua. Se
disuelven en solventes de baja polaridad.
|
es considerablemente más alta que
la de los alcanos
|
se disuelven en solventes no polares
|
Insoluble en agua, pero soluble en
solventes orgánicos no polares a 5,5°C.
|
||||||||||||
Propiedades Químicas
|
||||||||||||||||
Combustión
|
Combustión completa
|
Combustión completa
|
Combustión completa
|
|||||||||||||
Halogenación
|
dan origen a mezclas
de derivados halogenados, y desprendiendo halogenuros de
hidrógeno.
|
Se forma un compuesto cuyo nombre general
es dihalogenuro vecinal
|
Origina los tetrahaluros de alquilo.
|
Origina haluros de arilo
|
||||||||||||
Pirólisis
|
Se convierten en alcanos mas livianos,
alquenos y algo de hidrógeno
|
|||||||||||||||
Hidrogenación
|
Dan origen a alcanos
|
Forman un alqueno y luego el alcano
correspondiente
|
||||||||||||||
-
Son Combustibles
-
Poco Densos
-
Poco Hidrosolubles
-
Pueden ser de origen natural u origen sintético
-
Tienen carbono
-
Casi siempre tienen hidrogeno
-
Componen la materia viva
-
Constituyen una gran cantidad de sustancias existentes en la tierra
-
Presentan concatenación
Los compuestos orgánicos son utilizados
por el ser humano en su día a día, estos
constituyen la materia prima para la realización de una gran cantidad de productos.
Los alcanos, alquenos, alquinos y el benceno
poseen características que los diferencian entre
sí, pero que los diferencian de los compuestos
inorgánicos.
Isómeros Estructurales
Definición de isómeros
Se llaman isómeros a moléculas que tienen la misma formula molecular pero distinta estructura. Se clasifican en isómeros de cadena, posición y función.
Isómeros de cadena
Se distinguen por la diferente estructura de las cadenas carbonadas. Un ejemplo de este tipo de isómeros son el butano y el 2-metilpropano.
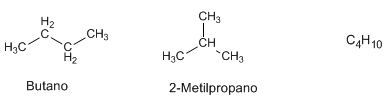
Isómeros de posición
El grupo funcional ocupa una posición diferente en cada isómero. El 2-pentanol y el 3-pentanol son isómeros de posición.
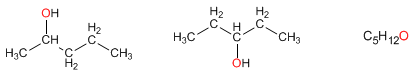
Isómeros de función
El grupo funcional es diferente. El 2-butanol y el dietil éter presentan la misma fórmula molecular, pero pertenecen a familias diferentes -alcohol y éter- por ello se clasifican como isómeros de función.
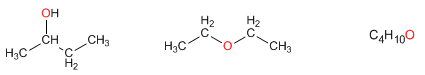
Se llaman isómeros a moléculas que tienen la misma formula molecular pero distinta estructura. Se clasifican en isómeros de cadena, posición y función.
Isómeros de cadena
Se distinguen por la diferente estructura de las cadenas carbonadas. Un ejemplo de este tipo de isómeros son el butano y el 2-metilpropano.

Isómeros de posición
El grupo funcional ocupa una posición diferente en cada isómero. El 2-pentanol y el 3-pentanol son isómeros de posición.

Isómeros de función
El grupo funcional es diferente. El 2-butanol y el dietil éter presentan la misma fórmula molecular, pero pertenecen a familias diferentes -alcohol y éter- por ello se clasifican como isómeros de función.

martes, 20 de mayo de 2014
Estimados alumnos de 4°C, este jueves 22/5 continuamos con el curso. Llevo los parciales, para discutir sobre los resultados y corrección. Solo los alumnos que obtuvieron 4 o 5 podrán realizar una prueba complemento recuperatoria el Lunes 26/5, en el horario normal de clase. Ese día ademas se dictara la clase para el resto de los alumnos.
Mensaje:
Mensaje:
- Felicitaciones a los que aprobaron! Solo queda la segunda prueba parcial.
- Ánimos a quienes deban dar la prueba complemento. Hay otra chance.
- Sigan los que perdieron el parcial, porque les aseguro que reglamentar es lo mas importante, ya que habrá una gran diferencia entre los exámenes reglamentados y los libres. Muchos temas no podrán ser dados por el poco tiempo que disponemos. No abandonen!
Dejo un fragmento del plan 92, para tener presente las pautas del mismo.
Fragmento del plan 92
Primera Prueba Parcial:
- En los cursos anuales, la primera Prueba Parcial se realizará en la segunda quincena de julio.
- En los cursos semestrales, la del 1er. Semestre se realizará en el mes de mayo y, la del 2º semestre, en setiembre.
- Consistirá en un trabajo escrito cuyos contenidos temáticos serán los de la primera parte del curso, comprendiendo por ella desde el inicio del curso a la fecha de realización de la prueba.
- Durante este período de pruebas parciales, se suspenderán los cursos regulares.
- Se confeccionará, centralmente, un Calendario que establezca horarios de Clases de Apoyo y de Prueba
- Primera Prueba Parcial – Complemento: Los alumnos que hubieren obtenido calificación 4 ó 5 en la Primera Prueba Parcial, tienen la posibilidad de realizar una Prueba Parcial Complementaria en un plazo no mayor a 10 en los cursos semestrales, o 20 días en los anuales después de haberse realizado la devolución de la misma.
- Segunda Prueba Sumativa:
- Para los cursos anuales se realizará durante la primera quincena del mes de octubre y, para los semestrales, será en el transcurso del último mes del curso. Se propondrán preferentemente trabajos escritos externos.
- En este período se continúa con los cursos regulares.
- Segunda Prueba Parcial (para eximidos de 1° año de Bachillerato) :
- Se realizará durante la última quincena o la última semana del curso, según el curso sea anual o semestral respectivamente.
- La prueba versará sobre los contenidos tratados en la segunda parte del curso (desde la Primer Prueba Parcial a la finalización del curso).
- eximidos=los que aprobaron la primera prueba parcial
lunes, 28 de abril de 2014
CUESTIONARIO PARA LA SUMATIVA (ENTREGAR COMO TD)
1)¿Cuál es la importancia del elemento
Carbono para los seres vivos?
2) ¿A qué se debe la gran diversidad de
compuestos que este elemento puede formar?
3) ¿Qué sustancia también es fundamental
para los seres vivos en la Tierra? Investiga acerca de sus características
químicas y expone en un texto al menos cinco de ellas.
4)¿En qué consiste el ciclo del carbono?
Explica con algún esquema y dibujos.
5) Qué es la combustión? ¿Por qué es tan
perjudicial para el equilibrio ambiental?
.............................................................................................................................
Suscribirse a:
Comentarios (Atom)


